Sie sind hier: Startseite > Harnblase > Neurogene Harninkontinenz > Diagnose und Therapie
Dranginkontinenz: Diagnose und Therapie
- Neurogene Harninkontinenz: Ursachen und Folgen
- Dranginkontinenz: Diagnose und Therapie
- Neurogene Harnblasenfunktionsstörungen: Therapie mit CIC, Botulinumtoxin A, Sakrale Neuromodulation und Operationen
Zusammenfassende Literatur neurogene Harninkontinenz: (Chapple u.a., 2005) (van Kerrebroeck, 1998) (Wein und Rackley, 2006). EAU Leitlinie: (Blok u.a., 2022).
Diagnose der Dranginkontinenz
Anamnese und körperliche Untersuchung:
- Fragebogen zur Intensität der Beschwerden wie z. B. IPSS.
- Miktionstagebuch
- Vorlagentest zur Quantifizierung der Inkontinenz
- Urologische und gynäkologische Untersuchung: Hinweise für eine Belastungsinkontinenz?
- Orientierende neurologische Untersuchung: Sensibilitätsprüfung für jedes (sakrale) Dermatom, Muskelkraftprüfung, Bizepssehnenreflex, Achillessehnenreflex, Patellarsehnenreflex, Babinski-Zeichen, Analreflex, Bulbocavernosusreflex, Kremasterreflex, Sphinktertonus.
- Fehlende Reflexantwort: bei akuter Schädigung des ersten Motorneuron (akutes Querschnittssyndrom) oder bei Schädigung der peripheren Nerven (Bandscheibenvorfall, Nervendurchtrennung).
- Gesteigertes Reflexniveau: bei chronischer Schädigung des ersten Motorneuron (Querschnittssyndrom, Apoplex), weitere Zeichen der Pyramidenbahnschädigung sind ein positives Babinski-Zeichen.
Laboruntersuchungen:
Urinsediment und Urinkultur, Serum-Kreatinin.
Sonographie:
Sonographie von Harnblase und Nieren: Harnstau? Dicke des Nierenparenchyms? Restharn? Harnblasenwanddicke?
Zystoskopie:
Die Zystoskopie ist weniger zur Diagnose der neurogenen Komponente notwendig, als zum Ausschluss von Differentialdiagnosen wie Tumoren, Zystitis oder Harnblasensteinen.
Miktionszysturethrographie:
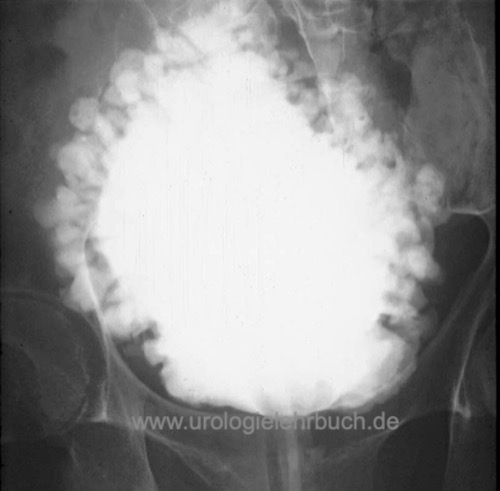
Die MCU wird meist im Rahmen der Urodynamik durchgeführt. Mögliche relevante pathologische Befunde sind eine verminderte Harnblasenkapazität, multiple kleine Divertikel (Abb. Christbaumblase), Restharn, Zeichen der subvesikalen Obstruktion oder vesikoureteraler Reflux.
Urodynamik:
Durch die klinische Symptomatik kann die Art der Störung nicht zuverlässig vorhergesagt werden, aber nicht alle Patienten benötigen eine urodynamische Diagnostik. Sie ist sinnvoll bei Patienten mit fehlendem Erfolg der konservativen Therapie, bei neurologischen Erkrankungen mit Gefahr der DSD und hohen Entleerungsdrücken und vor invasiver Therapie. Grundlagen und Durchführung der Urodynamik siehe Kapitel Urologische Untersuchungen/Urodynamik.
Differentialdiagnosen
Überaktive Harnblase, Dysfunktionale Miktion (Dysfunctional Voiding), BPH, Harnblasentumoren, Harnblasensteine, Infektionen wie akute Zystitis.
Therapie neurogener Harnblasenfunktionsstörungen
Verbesserung der Harnblasenspeicherfunktion bei Dranginkontinenz
Verhaltenstherapie:
Indikationen zur Verhaltenstherapie sind die milde Urgesymptomatik oder milde Dranginkontinenz. Die Verhaltenstherapie beinhaltet die Reduktion der Flüssigkeitszufuhr auf eine vernünftige Menge, Miktion nach festgelegten Zeitintervallen, Beckenbodengymnastik, Biofeedbacktherapie; oft in Kombination mit einer medikamentösen Therapie. Es kann eine Besserung in 50–70 % und eine Heilung in 15 % erwartet werden.
Anticholinerge Therapie bei Dranginkontinenz:
Anticholinergika wirken als Antagonisten auf muscarinerge Rezeptoren, dies führt zu einer Relaxierung der glatten Muskulatur [Kapitel Anticholinergika und ">Anatomie der Harnblase]. An der Harnblase wird die Kraft von normalen oder autonomen Detrusorkontraktionen gemindert und die funktionelle Harnblasenkapazität erhöht. Eine regelmäßige Miktion ist notwendig, um eine deutliche symptomatische Besserung zu erhalten. Ziel ist die Miktion bevor das Harnblasenvolumen, welches eine autonome Kontraktion induziert, erreicht ist. Die hohe Rate an störenden Nebenwirkungen führt häufig zur Absetzung der Therapie durch den Patienten. Eine intravesikale Therapie ist möglich und mit weniger Nebenwirkungen behaftet, ist aber nur bei Patienten mit intermittierendem Selbstkatheterismus sinnvoll. Folgende Substanzen werden hauptsächlich zur Therapie eingesetzt:
- Trospium: Dosierung 5 mg 1–1–1 bis 20 mg 1–1–1.
- Oxybutinin: Dosierung 2,5 mg 1–0–1 bis 5 mg 1–1–1–1.
- Tolterodin: Dosierung 1 mg 1–0–0 bis 2 mg 1–1–1. Retardpräparat mit 4 mg 1–0–0.
- Fesoterodin: Dosierung 4 mg 1–0–0, ggf. Steigerung auf 8 mg 1–0–0.
- Propiverin: 15 mg 1–0–1, ggf. Steigerung auf 1–1–1.
- Darifenacin: Dosierung 7,5–15 mg 1–0–0.
- Solifenacin: Dosierung 5–10 mg 1–0–0.
Botulinumtoxin A bei Dranginkontinenz:
Die transurethrale Injektionen von Botulinumtoxin A in den Detrusor führen zu einer passageren, mehrere Monate andauerenden Detrusorschwäche mit Erhöhung der funktionellen Harnblasenkapazität. Botulinumtoxin A ist indiziert bei Versagen oder Unverträglichkeit der anticholinergen Therapie (Cruz u.a., 2011). Die Dosierung (z. B. 100–300 Einheiten Botox) muss nach Wirkung und Nebenwirkung titriert werden, insbesondere wenn die Patienten spontan miktionieren. Bei zu hoher Dosierung besteht die Gefahr der Restharnbildung und der intermittierende Selbstkatheterismus (CIC) wird notwendig.
Weitere medikamentöse Therapieansätze:
β3-Rezeptor-Agonisten:
Adrenerge β3-Rezeptoren kommen auch in der Harnblase vor und vermitteln (kaum) kardiovaskuläre Wirkungen. Selektive β3-Rezeptoragonisten wie Mirabegron und Solabegron konnten sich in klinischen Studien als nebenwirkungsarme Therapieoption zur Therapie der überaktiven Harnblase beweisen. Mirabegron erhielt 2012 in den USA die Zulassung zur Therapie der überaktiven Harnblase. Die Dosierung beträgt 25 mg 1-0-0, ggf. Steigerung nach acht Wochen auf 50 mg 1-0-0. Die wichtigsten Nebenwirkungen in der Zulassungsstudie waren Übelkeit, Kopfschmerzen, Bluthochdruck, Durchfall, Verstopfung, Schwindel und Tachykardie (Nitti u.a., 2012). Langfristige Erfahrungen bezüglich der kardiovaskulären Sicherheit der β3-Rezeptorstimulation liegen noch nicht vor.
Sakrale Nervenmodulation:
die elektrische Stimulation der Hinterwurzel S3 führt zu einer Hemmung des Miktionsreflexes und damit zur Verminderung der autonomen Kontraktionen und Inkontinenz.
Indikation:
auf Medikamente nicht ausreichend ansprechende neurogene Detrusorüberaktivität. Vor Implantation des subkutanen Impulsgebers wird mit Hilfe einer mehrtägigen perkutanen Testung der potentielle Therapieerfolg getestet.
Ergebnisse:
Bei 50 % der Patienten wurde nach perkutaner Testung der Impulsgeber implantiert. Bei einer Nachbeobachtung über 4 Jahre konnten davon 40 % geheilt werden, bei weiteren 20 % konnte eine Symptomverbesserung erzielt werden.
Perkutane afferente Neuromodulation:
die wöchentliche Reizung des N. tibialis über eine perkutane Nadel am Knöchel führt zu einer Symptomverbesserung in 60 %.
Harnblasendenervierung:
die Harnblasendenervierung existiert in verschiedenen Techniken mit Durchtrennung von Nerven auf spinaler oder peripherer Ebene. Die Techniken sind aufgrund besserer Alternativen in den Hintergrund der therapeutischen Bemühungen getreten, seltene Indikation sind z.B. die schwere autonome Dysreflexie. Problematisch sind die Nebenwirkungen auf andere Organsysteme (Rektum, Sensibilität) und die Regeneration des Nervensystems (Neuroplastie) mit vielleicht schlechterer Funktion.
Harnblasenaugmentation:
Das Ziel der Harnblasenaugmentation ist die Vergrößerung der Harnblasenkapazität. Bei erhaltener Kontrolle über den Harnblasensphinkter sind gute Ergebnisse zu erwarten. Postoperativ kann Restharn entstehen, der Patient sollte in der Lage sein, Selbstkatheterismus (CIC) durchzuführen. Ein postoperativer Harnverhalt mit niedrigen Füllungsdrücken und Notwendigkeit der CIC istd jedoch deutlich besser für den Patienten als eine Detrusorhyperreflexie mit hohen Miktionsdrücken und Gefahr der Nierenschädigung. Zahlreiche Techniken der Harnblasenaugmentation existieren:
- Harnblasen(auto)augmentation mit Erhalt des Urothels (Detrusormyotomie)
- Harnblasenaugmentation mit Darm (Magen, Ileum, Kolon)
- Harnblasenaugmentation mit Ureter, wenn ein stark dilatierter Ureter einer funktionslosen Niere verfügbar ist.
| Neurogene Harninkontinenz 1/3 | Suchen | Neurogene Harninkontinenz 3/3 |
Sachregistersuche: A B C D E F G H I J K L M N O P Q R S T U V W X Y Z
Literatur
Abrams, P.; Cardozo, L.; Fall, M.; Griffiths, D.; Rosier, P.; Ulmsten, U.; van Kerrebroeck, P.; Victor, A.; Wein, A. & of the International Continence Society, S. S. The standardisation of terminology of lower urinary tract function: report from the Standardisation Sub-committee of the International Continence Society.Neurourol Urodyn, 2002, 21, 167–178.
Chapple u.a. 2005 CHAPPLE, C. ; KHULLAR, V. ; GABRIEL, Z. ; DOOLEY, J. A.: The effects of antimuscarinic treatments in overactive bladder: a systematic review and meta-analysis.
In: Eur Urol
48 (2005), Nr. 1, S. 5–26
Cruz, F.; Herschorn, S.; Aliotta, P.; Brin, M.; Thompson, C.; Lam, W.; Daniell, G.; Heesakkers, J. & Haag-Molkenteller, C. Efficacy and safety of onabotulinumtoxinA in patients with urinary incontinence due to neurogenic detrusor overactivity: a randomised, double-blind, placebo-controlled trial.
Eur Urol, 2011, 60, 742-750
Gauruder-Burmester, A.; Wildt, B. & Tunn, R. [Treatment of overactive bladder with sodium chondroitin sulphate].
Zentralbl Gynakol, 2006, 128, 336-340.
van Kerrebroeck 1998 KERREBROECK, P. E. V. van:
Neurogenic Bladder Dysfunction.
In: Eur Urol
Curric Urol 4.2 (1998), S. 1–9
Nitti, V.; Auerbach, S.; Martin, N.; Calhoun, A.; Lee,
M. & Herschorn, S.
Results of a Randomized Phase III Trial of
Mirabegron in Patients with Overactive Bladder.
J Urol, 2012.
Wein und Rackley 2006 WEIN, A. J. ; RACKLEY,
R. R.:
Overactive bladder: a better understanding of pathophysiology,
diagnosis and management.
In: J Urol
175 (2006), Nr. 3 Pt 2, S. S5–10